کیمیاگران قرن 21
سوالات کنکور و دانشگاهی- نکات اخلاقی و پندآموز- روشهای تحقیقی- اطلاع رسانیهای مختلفکیمیاگران قرن 21
سوالات کنکور و دانشگاهی- نکات اخلاقی و پندآموز- روشهای تحقیقی- اطلاع رسانیهای مختلفچند آزمایش آتش زا در آزمایشگاه
ترکیب مشهور پتاسیم پرمنگنات و گلیسیرین:
مقداری پتاسیم پرمنگنات (KMnO4) به عنوان اکسنده و گلیسیرین (C3H5(OH)3) به عنوان سوخت را به نسبت 3 به 1 روی هم میریزیم (اول پرمنگنات را به صورت کوه در می آوریم و چاله ای در آن ایجاد می کنیم. سپس گلیسیرین را داخل چاله می ریزیم.) حالا از یک حقه ی قدیمی استفاده کرده روی کوه مقداری آب میریزیم. البته تف بهتر جواب می دهد ولی ممکن است واکنش جلوی صورتتان رخ دهد یا با کمی پرمنگنات دهنتان را شیرین کنید. (من خودم در این زمینه تجربه دارم. پرمنگنات واقعا شیرین است ولی اصلا توصیه نمی کنم آن را مزه کنید!)
14KMnO4 + 4C3H5(OH)3 --> 7K2CO3 + 7Mn2O3 +5CO2 +16H2O
آمونیم نیترات و روی با (آب و الکل) یا هیدروکلریدریک اسید:
آمونیم نیترات (NH4NO3) با روی (Zn) و کمی نشادر (آمونیوم کلرید – NH4Cl) با آب یک دودزا تولید می کنند که هم شعله و هم حرارت زیاد دارد. کافی است مواد را با با نسبت های آمونیم نیترات 5، روی 3 و نشادر 2 قسمت جرمی را با هم ترکیب کرده و به آن محلول آب و اتانول (به نسبت 1 به 1 حجمی) را به آن بیافزایید. آتش میگیرد ولی دودش سمی است.همین طور می توانید به جای آب هیدروکلریدریک اسید (HCl) بیافزایید. در این آخری در اوایل واکنش به علت تولید HCl(البته هیدروکلریدریک اسید محلول این گاز در آب است که در اثر حرارت از حالت محلول در می آید. این جا هم جنین اتفاقی می افتد.) دود حاصل، اسیدی است.
دلیل این واکنش ها این است که آمونیم نیترات با الکل و هیدروکلریدریک اسید واکنش میدهد. روی و آمونیم نیترات با رطوبت انرژی فعال سازی خود را گرفته و واکنش را اغاز می کنند. این رطوبت معمولا از رطوبت هوا گرفته میشود. پس آب کاتالیزگر است. روی هم در این واکنش سوخت است. الکل و هیدروکلریدریک اسید هم با آمونیم نیترات واکنش می دهند.
پتاسیم کلرات و شکر و اسید سولفوریک
به این صورت که پتاسیم کلرات (KClO3) جز اکسنده را پودر کرده و آن را با شکر (C12H22O11) به عنوان سوخت با نسبت 5 به 3 ترکیب می کنیم. دقت کنید می توانید از نسبت های 3 به 2 هم استفاده کنید. مواد را مثل کوه کرده و وسط آن چالهای ایجاد می کنیم. سپس چند قطره اسید سولفوریک (H2SO4) را با فاصله به روی چاله اضافه می کنیم.
سدیم پراکسید و روی یا پوشال چوب و آب
سدیم پراکسید (Na2O2) یک اکسنده به شکل بلور های بی بو و زرد کمرنگ است. این ماده هم مثل سدیم با آب واکنش میدهد.
هشدار: سدیم پراکسید هرگز نباید با پوست تماس پیدا کند زیرا سبب سوختگی می شود.
بهتر است این آزمایش را در بشر انجام ندهید چون ممکن است باعث ترک خوردن بشر یا شکستن آن شده و ذرات شیشه را به اطراف پرت کند. همین طور می توانید به چای پوشال از پودر روی استفاده کنید.
اسید سولفوریک و پتاسیم پرمنگنات
در واقع ما با ترکیب اسید سولفوریک و پرمنگنات، منگنز هپتاکسید (ماده اکسنده – MnO7) می سازیم. پرمنگنات و سولفوریک اسید را طوری باهم ترکیب کنید که مایع غلیظی حاصل شود. حالا هر ماده ای که خاصیت اشتعال پذیری دارد، در تماس با این ترکیب می سوزد. مثل: چوب، کاغذ، استون ، فیتیله یا ... در واقع این ترکیب در صورت تماس با ماده اشتعال پذیر دما را بالا برده و سبب می شود جسم مورد نظر انرژی فعال سازی خود را بگیرد. اگر اسم ترکیب منگنز هپتاکسید و استون را شنیدید، ان هم از این دسته است چرا که همان طو که گفته شد این ماده با استون هم واکنش می دهد. حتی می توانید روی کاغذ آغشته به استون منگنز هپتاکسید خود را بریزید. اما من تا حالا این کا رو نکردم. مُردید به من ربطی نداره.
تجربه سال 93: می خواستم با اکسید کردن ایزوپروپیل الکل آن را به کتون و بعد تحت اکسایش سخت به کربوکسیلیک اسید (2-پروپانوییک اسید) تبدیل کنم. اما اسید را رقیق نکردم و موقع اضافه کردن الکل در بشر آتش سوزی به راه افتاد و بخاری سبز رنگ تولید شد که 100% به علت وجود ترکیبات منگز دار است.ر
فرمول محاسبه تراز در کنکور ها و آزمون ها
فرمول محاسبه ی تراز در کنکورها و آزمون ها
شاید برایتان پیش آمده باشد که معنی و مفهوم کلمه ی [ تراز ] چیست ! اصلا چرا تراز مهم است ؟ تراز به چه درد میخورد ! و چرا در کنکور ها و آزمون ها و گاها امتحانات تستی از آن استفاده میشود !
از هر کس هم میپرسی جواب میدهد » هر چه تراز بالاتر بهتر ! ( خیلی ممنون واقعا :| )
کنکور۱۰۰ برای پاسخی کامل برای شما عزیزان داوطلب کنکوری و کسانی که دوست دارید بدانید تراز چیست آماده کرده است با ما همراه باشید .
چرا تراز اهمیت دارد؟
خب، برای اینکه افراد یک آزمون را رتبهبندی کنیم، شما چه راهی پیشنهاد میکنید؟
خوب، ممکن است بگویید هر کس هر نمرهای که صرفا گرفت (که اصطلاحاً آنرا «نمره خام» مینامیم) در رتبه بالاتری قرار بگیرد.
خوب، با این حساب مثلاً شما نمره ۱۷ میگیرید و در جایگاه اول قرار میگیرید اما فردای همان روز یک آزمون دیگر گرفته میشود و شما در آن آزمون هم ۱۷ میگیرید اما این بار در جایگاه آخر قرار میگیرید. چرا؟ چون دیروز سؤالات آسان بوده و امروز سؤالات سخت.
متوجه میشوید مشکل چیست؟ نمره ۱۷ شما یک بار ارزش بالاترین را داشت و یک بار ارزش پایینترین! یعنی بحث این است که مثلاً ممکن است من در کنکور امسال نمرهام ایکس بشود و نفر اول کنکور بشوم. بعد کنکوریهای سالهای قبل بگویند چون آزمون آسان بوده ایشان نمره بالا گرفته و از این جور حرفها…
یا مثلاً ممکن است شما ریاضی که درس با ضریب بالا است را خوب بزنید و نمره خوبی بگیرید اما در درس ادبیات هیچ دانشی نداشته باشید!
یک مشکل دیگر که تراز حل میکند این است: فرض کنید بخواهیم بر اساس «نمره خام» رتبهبندی کنیم. فرض کنید یک نفر در یک کلاس ۱۸ گرفته. آیا میشود گفت او نفر اول میشود؟ خیر! شاید آزمون آنقدر ساده بوده که همه افراد کلاس ۱۹ و ۲۰ گرفتهاند و او آخرین نفر میشود! یعنی ۱۸ آن ارزشی که در آزمونهای دیگر دارد را ندارد!
در بحث «تراز» (یا Balance) ما دنبال «یکسانسازی ارزش نمره» و «نرمالسازی» (Normalization) هستیم. یعنی ترازی که میگیرید همیشه ارزشش همان باشد و اینکه نسبت به «همه سؤالات» سنجیده شوید. در ترازبندی، تکتک سؤالات مهم میشوند (یعنی هر چه دیگران به آن سؤال، کمتر پاسخ صحیح دهند، ارزشش آن سؤال بالاتر میرود) و اینکه سطح بقیه افراد چطور باشد، روی تراز شما مؤثر است.
تراز، معمولاً عددی است بین ۰ تا ۱۰۰۰۰ و ظاهراً گاهی اوقات روی ۱۵۰۰۰ هم تنظیم میکنند. (بسته به تعداد شرکت کنندگان)
فرمول به دست آوردن تراز هر درس چیست؟
برای به دست آوردن تراز کلی داوطلب ابتدا باید تراز او در هر درس را به دست آوریم.
تراز کاربر در هر درس طبق فرمولهای زیر محاسبه میشود
نمره خام در کنکور و آزمونهای مشابه چطور محاسبه میشود؟
همانطور که میبینید برای محاسبه تراز، به «نمره خام» نیاز دارید. نمره خام همان است که شما بارها شنیدهاید: اگر آزمون نمره منفی داشته باشد، باید تعداد گزینههای صحیح را بشماریم و به ازای هر ۳ غلط یکی از تعداد صحیحها کم کنیم. سپس عدد را به تعداد کل سؤالات تقسیم کنیم و نتیجه را در ۱۰۰ ضرب کنیم تا یک عدد درصدی به دست آید. این میشود نمره خام شما در آن درس.
مثلاً اگر از ۲۵ سؤال، ۱۰ سؤال را صحیح بزنید و ۳ سؤال را غلط و بقیه را نزنید، نمره خام شما میشود:
(۱۰-۱)/۲۵*۱۰۰=۳۶%
شاید فرمول راحتتر این باشد:

True : تعداد پاسخهای صحیح
False : تعداد پاسخهای غلط
Total : تعداد کل سؤالات
فرمول به دست آوردن تراز کل چیست؟
برای به دست آوردن تراز کل، اینطور که یک جا نوشته شده، باید تراز هر درس را ضربدر ضریب آن کنید و با هم جمع کنید. سپس نتیجه را تقسیم بر جمع ضرایب دروس کنید. یعنی:
![]()
هر چند من در تستا طبق این فرمول عمل کردم اما فکر میکنم تراز کل هم باید مانند همان تراز هر درس حساب شود. یعنی باید نمره خام میانگین را برای کل آزمون به دست آوریم. سپس سیگمای تفریق نمره خام همه داوطلبین منهای نمره میانگین و ادامه ماجرا…
این را هنوز مطمئن نیستم. اگر کسی از دوستان میداند و مطمئن است لطفاً در بخش نظرات اعلام کند.
برگرفته از وبلاگ دکتر حجتی
محاسبه سریع تعداد مولکول های ممکن از ایزوتوپ ها
محاسبهی سریع تعداد مولکولهای ممکن از ایزوتوپها
سلام
برخی وقت ها دنبال راه حل سریع برای حل برخی مسائل میگردیم. مثلا میخواهیم تعداد مولکولهای نیتریک اسید ممکن که از سه ایزوتوپ هیدروژن و دو ایروتوپ اکسیژن و دو ایزوتوپ نیتروژن را بدست بیاوریم. در این صورت با کمک ریاضی می توان فرمول مفیدی بدست آورد.
اگر
تعداد ایزوتوپها = k
تعداد اتمها در فرمول = n
فرض میکنیم.
برای دو اتم i و j تعداد کل فرمولهای ممکن از رابطهی زیر بدست میآید:
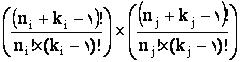
منظور از ! فاکتوریال است. مثلا 2×3×4×5×6×7×8=!8
مثال1: با سه ایزوتوپ هیدروژن و دو ایزوتوپ اکسیژن چند نوع مولکول هیدروژن پراکسید بدست میآید؟
6 12 18 24
جواب: 18
برای هیدروژن پراکسید (که نام صحیح آن دی هیدروژن دی اکسید است زیرا یک ترکیب مولکولی است نه یونی) با فرمولH2O2 در صورتی که سه ایزوتوپ هیدروژن (i) و دو ایزوتوپ اکسیژن (j) باشد خواهیم داشت:
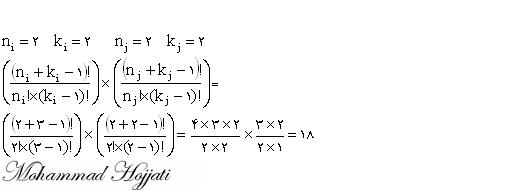
اما اگر مساله تعداد مولکولها که جرم مولی متفاوت دارند را خواسته باشد حل آن کمی راحتتر است. چون برخی از مولکولهای هیدروژن پراکسید که از ایزوتوپهای غیر یکسانی از هیدروژن و اکسیژن تشکیل شده اند جرم مولی برابر دارند و از آنجا که جرم مولی را میتوان از روی عدد جرمی بدست آورد پس با یک عدد صحیح ( بخوانید غیر اعشاری ) سر و کار داریم یعنی اختلاف جرم های این مولکول ها عدد صحیح است پس کافی است اختلاف سنگین ترین مولکول ممکن و سبک ترین آن ها را محاسبه کرد و عدد یک را به آنها افزود.
مثال2: با سه ایزوتوپ هیدروژن و دو ایزوتوپ اکسیژن 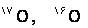 ) چند مولکول هیدروژن پراکسید با جرم مولی متفاوت بدست میآید؟
) چند مولکول هیدروژن پراکسید با جرم مولی متفاوت بدست میآید؟
1) 4 2) 7 3) 10 4) 18
نکته حیاتی: ایزوتوپ های هیدروژن را باید حفظ نمود در خاطر مبارک!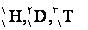 که نام فامیلی مشترک اما نام کوچک متفاوت دارند اولی را پروتیم ، دومی را دوتریم و آخری که خیلی خطرناک است ( آروم بخوانید) تریتیم نام دارد (پرتوزا است. یواش).
که نام فامیلی مشترک اما نام کوچک متفاوت دارند اولی را پروتیم ، دومی را دوتریم و آخری که خیلی خطرناک است ( آروم بخوانید) تریتیم نام دارد (پرتوزا است. یواش).
فرمول مورد استفاده:
تعداد کل حالات ممکن={1+ [جرم مولی سنگین ترین مولکول] - [جرم مولی سنگین ترین مولکول]}
سنگین ترین مولکول
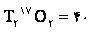 سبک ترین مولکول
سبک ترین مولکول
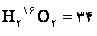 7=1+34-40ر
7=1+34-40ر
برگرفته از وبلاگ دکتر حجتی
